"Acho que em qualquer época eu teria amado a liberdade; mas na época em que vivemos, sinto-me propenso a idolatrá-la"
(Tocqueville)
Uso de medicamentos em fase de teste é aceito pelos parâmetros internacionais durante surtos pandêmicos
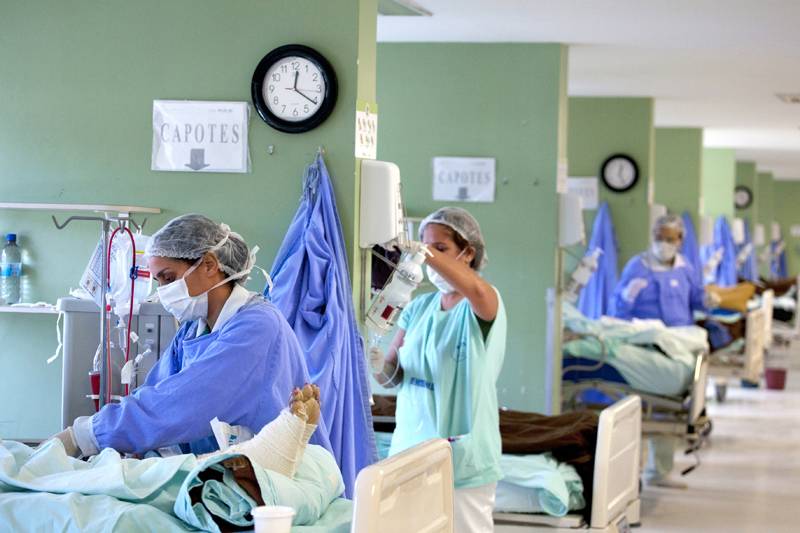
Em tempos de normalidade, a colocação de um remédio no mercado exige a demonstração de sua qualidade, segurança e eficácia, comprovadas por métodos altamente exigentes.
Durante surtos pandêmicos de novas doenças, no entanto, a lógica não é a mesma.
É que, conforme reconhece o próprio site da ANVISA, o iter de autorização de uma nova medicação exige testes que podem levar um tempo muito longo. Logo, incompatível com a premência exigida por uma doença nova, e que portanto avança muito rápido sem encontrar grupos imunizados e para a qual ainda não há tratamentos.
Na ANVISA, como ocorre também em outros lugares, a autorização possui várias etapas. Apenas uma delas, a chamada “fase clínica”, a qual tem “por objetivo investigar o funcionamento e a segurança do medicamento nos seres humanos”, é dividida em várias fases “que podem durar muitos anos”.
Assim, segundo documento elaborado pela Organização Mundial da Saúde em 2016, o “Guia para o Gerenciamento de Questões Éticas em Surtos de Doenças Infecciosas” (Guidance For Managing Ethical Issues In Infectious Disease Outbreaks), aponta diretrizes distintas e menos exigentes para o que chama de “uso emergencial de intervenções não comprovadas fora do contexto de pesquisas”, objeto do item 9 do documento.
Existem doenças infecciosas (pathogens) para as quais não existe intervenção eficaz exaustivamente comprovada. Para algumas delas, todavia, pode haver intervenções que tenham demonstrado segurança e eficácia promissoras em laboratório e em modelos animais relevantes, mas que ainda não foram avaliadas quanto à segurança e eficácia em humanos. Em circunstâncias normais, tais intervenções passariam por testes em ensaios clínicos capazes de gerar evidências confiáveis sobre sua segurança e eficácia. No entanto, no contexto de um surto caracterizado por alta mortalidade, pode ser eticamente apropriado oferecer intervenções experimentais a pacientes individuais em caráter emergencial fora ensaios clínicos (…).
É o que se chama de “uso compassivo” de medicamentos. A medida foi inclusive autorizada pela própria OMS durante a crise deflagrada pelo Ebola.
O documento da OMS aponta alguns requisitos para esse tipo de expediente:
a) não deve haver alternativa com eficácia já comprovada;
b) inviabilidade de aguardar os testes clínicos;
c) os dados preliminares têm de indicar que os benefícios superam os riscos;
d) autoridades públicas ou comitês qualificados admitam o uso;
e) deve haver meios disponíveis de minimizar os riscos associados;
f) o uso deve ser monitorado e os resultados registrados;
g) o paciente deve consentir após ser devidamente informado e esclarecido sobre os efeitos e riscos do medicamento e sobre suas alternativas.
O médico Fabrizio Prado, da Universidade Estadual de Londrina, afirma que o uso de medicamentos em fase de testes no decorrer de surtos epidêmicos é algo já consagrado na bioética. Não é, portanto, apenas uma questão de o documento da OMS prever. O documento simplesmente reconhece uma prática correta e já aceita de modo geral.
Essas lições são extremamente úteis hoje no Brasil, em virtude das discussões acerca do uso do “coquetel” contra o coronavírus chinês, composto por hidroxocloroquina, azitromicina e zinco.
Embora essa combinação não tenha passado por todos os testes para que pudesse ser comercializada em períodos de normalidade, diante do quadro pandêmico e urgente por nós enfrentado, ela pode ser ministrada, pois satisfaz as exigências acima.
Com efeito, não existe hoje alternativa que tenha satisfeito os níveis testes mais exigentes para combate ao coronavírus.
É inviável aguardar testes clínicos segundo os métodos mais exigentes, em virtude da velocidade e mortalidade relativamente alta da doença.
Vários estudos levados a cabo até qui dão conta do sucesso do coquetel no combate à doença, principalmente quando administrado de maneira precoce, segundo protocolo utilizado pela Prevent Senior.
O protocolo para usa do coquetel vem sendo adotado nas últimas semanas por alguns dos principais hospitais de São Paulo — como a Santa Casa, o Albert Einstein e o Sancta Maggiore, além de estar sendo utilizado também em outros lugares do mundo, como França e Estados Unidos.
Os riscos associados a esses medicamentos são completamente conhecidos, visto que já são aplicados no Brasil há anos.
O resultados estão sendo devidamente acompanhados e registrados.
Resta apenas a obrigatoriedade de sempre alertar ao paciente sobre os efeitos conhecidos, seu grau de certeza, os riscos e alternativas. O coquetel poderá, assim, ser aplicado somente de forma condicionada ao consentimento informado e esclarecido.
O médico Dr. Fabrizio Prado esclarece que conceder, diante do nível de evidência atual, o direito de o paciente decidir “é respeitar sua autonomia e liberdade, podendo ele por si mesmo, baseado nas informações dadas, analisar o risco/benefício e escolher sobre aquilo que ele quer na sua vida. Isso vai justamente contra a medicina paternalista e protecionista que não tem mais lugar hoje em dia”.
Ele também afirma que, embora seja necessário “haver pesquisas sérias para a busca de evidências, as duas coisas podem ocorrer em paralelo em locais diferentes”. Ou seja, o uso compassivo não é uma alternativa excludente em relação à continuidade das pesquisas.
Logo, pode-se concluir como perfeitamente possível, do ponto de vista da ética médica e do direito aplicável, o uso em larga escala, inclusive de modo precoce, do coquetel contra o coronavírus.


deixe sua opinião